Sheila Kooderings Clemens-Hemmer is Verpleegkundig Specialist AGZ – Hartfalen in het Rijnstate ziekenhuis in Arnhem. Sheila is één van de schrijvers van de kennismodule “handreiking Cardiotoxiciteit” die voor het netwerk verpleegkundig specialisten oncologie is gemaakt.
Door Sheila haar bijdrage aan deze kennismodule is de belangstelling voor cardiotoxiciteit gerelateerd aan oncologie (behandeling) versterkt.
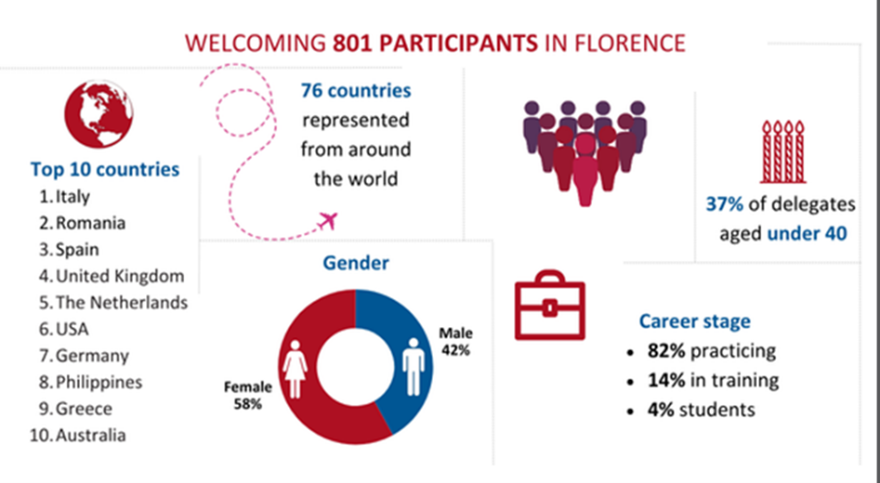
Daarom heeft ze in juni 2025 het ESC Cardio-oncology congres in Florence bezocht.
In dit verslag de highlights van Sheila en haar take-home messages.
De algemene indruk is dat het een interessant congres is. Zowel de mooie en hoopgevende onderzoeksresultaten als de presentatie van de “Clinical Cases” maakten duidelijk dat cardiotoxiciteit veelomvattend is.
Steeds meer patiënten zijn inmiddels zowel oncologische als cardiologische patiënt. Dit congres maakte duidelijk dat samenwerking daarom erg belangrijk is: Je wilt als behandelaren de beste oncologie behandeling kunnen (blijven) geven door het cardiovasculair risico (cv-risico) te minimaliseren. Dit vraagt om een proactieve aanpak in plaats van een reactieve aanpak, zoals nu vaak nog het geval is. Het blijft tegelijkertijd ook balanceren tussen praktische haalbaarheid en cardiotoxiciteit (CT).
Cardiotoxiciteit gaat duidelijk verder dan alleen hartfalen. De Clinical Cases waren bijzonder leerzaam en zorgden voor nieuwe inzichten. Zo kwam naar voren dat het proactief inzetten van ACE-remmers en bètablokkers bij geselecteerde patiënten, in combinatie met opvolging via TTE en ECG, ervoor kan zorgen dat een kankerbehandeling veilig kan doorgaan zonder onderbreking van de oncologische therapie. Multidisciplinaire samenwerking speelt hierbij een cruciale rol om de uitkomsten voor patiënten te verbeteren. Daarnaast kan intensievere samenwerking er ook toe bijdragen dat zorgverleners elkaars taal beter leren begrijpen, wat momenteel nog vaak een uitdaging vormt.
Soms bestaan er ook alternatieve behandelingen voor bijv. antracyclines bij high-riskpatiënten, maar die geven dan weer kans op hematologische bijwerkingen.
Er zijn situaties waarbij binnen een categorie van oncolytica gekozen kan worden voor een middel dat een veel beter risicoprofiel geeft. Zoals bijvoorbeeld fluoropyrimidines bij vaatspasmen.
Belangrijk om je te realiseren is dat niet alleen de kanker, maar vaak het hele systeem van de patiënt de kans op CT vergroot (sexe, RF, cardiovasculaire voorgeschiedenis bijv.) De prognoses van patiënten met deze risicofactoren is beduidend minder goed en daarom is patiënten-educatie over de leefstijl en risico’s bij deze patiënten mogelijk nog belangrijker. Verpleegkundigen en verpleegkundig specialisten kunnen binnen de rol die ze in de multidisciplinaire behandeling hebben ook hierin een belangrijke bijdrage leveren door patiënten hierover voor te lichten en zo nodig begeleiding te bieden.
Onderzoek
Ook interessant op dit congres waren de lopende onderzoeken zoals:
- MRI op varkens waaruit blijkt dat myocardiaal oedeem een voorteken lijkt te zijn van CT. Dit kan mogelijk in de toekomst dus nuttig zijn met name wanneer je hoge doses antracyclines wil geven. Zou in de toekomst kunnen betekenen: bij high-riskpatiënten vooraf een MRI uitvoeren en als er geen oedeem te zien is, is het veilig om hoger dosis te geven (dit moet dus nog bewezen worden!).
- Verder is het fijn dat er steeds meer tools komen zoals apps om de risico-inschatting mee te maken.
- Prostaatkankerbehandeling geeft een grotere kans op atherosclerose. Mogelijk is het verstandig om preventief een statine te starten.
- Zowel statines als SGLT2i laten in studies bij borstkanker zien dat ze positieve uitkomsten geven als je met deze middelen start 7 dagen voor aanvang van de antracyclines. (Empacard pilot trial –> significant minder afname van Ejectiefractie (EF) van GLS* bij SGLT2i dan placebo).
- Er is een ontwikkeling gaande dat bij chronische leukemie bijvoorbeeld de behandeling veranderd van chemotherapie naar targettherapie (BTKi). Het gevolg is dat er meer risico op cardiale fibrose en aritmieën (als AF), hypertensie en bloeding is dan bij de conventionele therapie.
- Patiënten met kanker hebben 2 x zoveel risico op MI en stroke. Dit wordt veroorzaakt door inflammatie en door de middelen die bij de oncologische behandeling wordt ingezet. Acuut coronair syndroom (ACS) patiënten met kanker hebben slechtere uitkomsten doordat we ze minder vaak goed revasculariseren door een dotter of bypassbehandeling. Meningen zijn hierover verdeeld. Er kan een terughoudendheid zijn door bloedingsriscio. Meest bij colonkanker. Patiënten met kanker hebben kans op trombocytopenie tijdens actieve kankerbehandeling. Bij NSTEMI ziet men geen verschil in mortaliteit tussen wel/geen revascularisatie bij actief kanker. Overweging zou kunnen zijn om al preventief statine in te zetten als er op de CT al kalk te zien is in de coronair vaten. Dit wordt nu nog weinig gedaan.
- Patiënten met hartfalen kunnen ook kanker krijgen. Dit heeft impact op de opties van behandelen zowel oncologisch als cardiologisch. Daarbij kunnen de specialismen elkaar helpen met de best passende behandeling waarbij de bijwerkingen en effecten van de behandeling goed gewogen kunnen worden.
De conclusie is dat het een interessant congres is, waar je in de praktijk iets aan hebt. En dat er nog wel het een en ander te doen is op het gebied van kwaliteit van zorg aan deze patiëntengroep.
Het congres is volgend jaar in Wenen en is een aanrader voor zowel oncologen, cardiologen en de Verpleegkundig Specialisten (en verpleegkundigen) in deze vakgebieden. Samengaan met je collega’s uit het andere specialisme kan zeer waardevol zijn.
Door samen te werken vanuit de 2 specialismen kunnen we van stoppen van de oncologische behandeling van deze cardio-onco patiënten naar veilig behandelen op beide vlakken realiseren en dat is pure winst.
* GLS afname: Global Longitudinal Strain afname, verwijst naar een verminderd rekvermogen van de linkerhartkamer.